خلية دانيال - تحويل الطاقة الكيميائية الى طاقة كهربية скачать в хорошем качестве
Повторяем попытку...
Скачать видео с ютуб по ссылке или смотреть без блокировок на сайте: خلية دانيال - تحويل الطاقة الكيميائية الى طاقة كهربية в качестве 4k
У нас вы можете посмотреть бесплатно خلية دانيال - تحويل الطاقة الكيميائية الى طاقة كهربية или скачать в максимальном доступном качестве, видео которое было загружено на ютуб. Для загрузки выберите вариант из формы ниже:
-
Информация по загрузке:
Скачать mp3 с ютуба отдельным файлом. Бесплатный рингтон خلية دانيال - تحويل الطاقة الكيميائية الى طاقة كهربية в формате MP3:
Если кнопки скачивания не
загрузились
НАЖМИТЕ ЗДЕСЬ или обновите страницу
Если возникают проблемы со скачиванием видео, пожалуйста напишите в поддержку по адресу внизу
страницы.
Спасибо за использование сервиса ClipSaver.ru
خلية دانيال - تحويل الطاقة الكيميائية الى طاقة كهربية
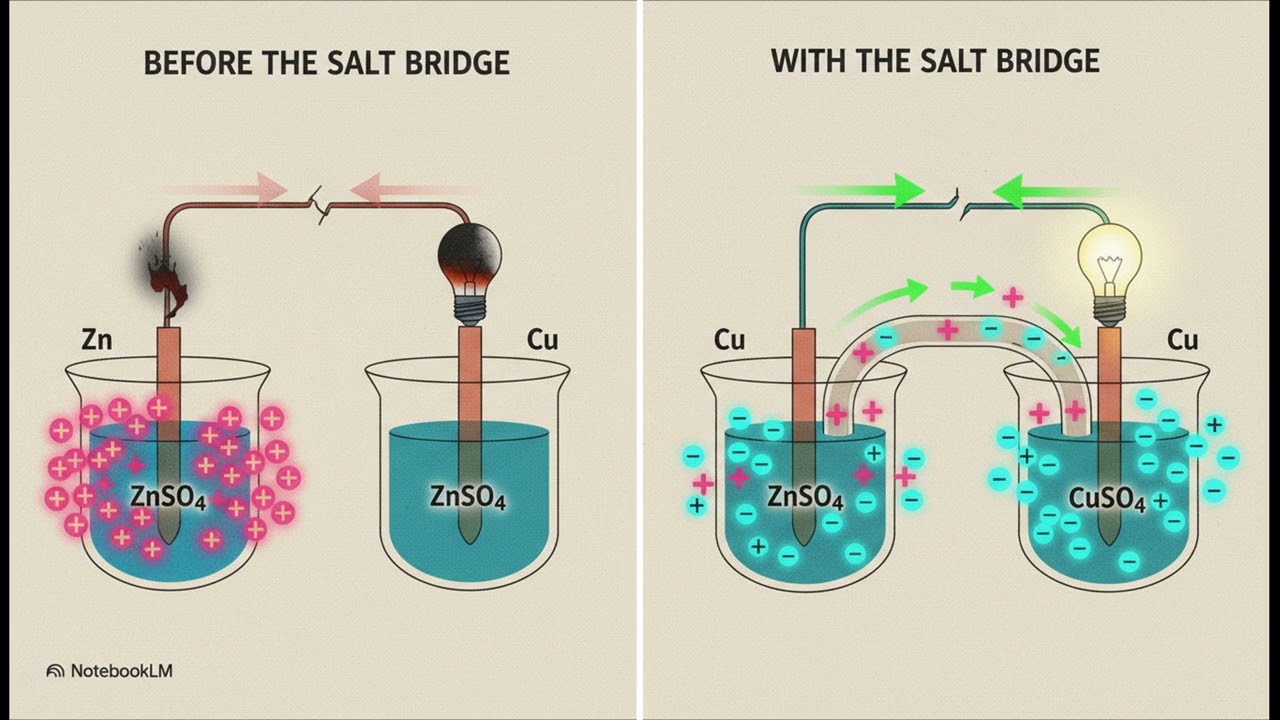
*خلية دانيال* (Daniell Cell) هي نوع من *الخلايا الكهروكيميائية* (الجلفانية) التي تعمل على *تحويل الطاقة الكيميائية إلى طاقة كهربائية* من خلال تفاعلات أكسدة واختزال تلقائية [68، 115]. إليك شرح مفصل لمكوناتها وآلية عملها بناءً على المصادر: *1. مكونات الخلية* تتكون خلية دانيال من نصفي خلية موصولين ببعضهما [22، 68]: *المصعد (الأنود):* هو القطب السالب، ويتكون من لوح من *الخارصين (الزنك)* مغمور في محلول كبريتات الخارصين ($ZnSO_4$) [68، 22، 117]. *المهبط (الكاثود):* هو القطب الموجب، ويتكون من لوح من *النحاس* مغمور في محلول كبريتات النحاس ($CuSO_4$) [68، 23، 117]. *الجسر الملحي (القنطرة الملحية):* أنبوبة زجاجية على شكل حرف U تحتوي على محلول إلكتروليتي لا يتغير كيميائياً (مثل الأجار)، وتعمل على *نقل الأيونات* بين المحلولين للمحافظة على *التعادل الكهربائي* وإكمال الدائرة [68، 118، 23]. *2. التفاعلات الكيميائية* تحدث داخل الخلية التفاعلات التالية [69، 117]: *تفاعل الأكسدة (عند المصعد):* تفقد ذرات الخارصين إلكترونات وتتحول إلى أيونات تذوب في المحلول. $Zn(s) \rightarrow Zn^{2+}(aq) + 2e^-$ *تفاعل الاختزال (عند المهبط):* تكتسب أيونات النحاس الموجودة في المحلول الإلكترونات القادمة من المصعد وتترسب كذرات نحاس صلبة. $Cu^{2+}(aq) + 2e^- \rightarrow Cu(s)$ *التفاعل الكلي للخلية:* $Zn(s) + Cu^{2+}(aq) \rightarrow Zn^{2+}(aq) + Cu(s)$ *3. آلية العمل وانتقال الطاقة* تتولد الإلكترونات عند المصعد وتنتقل عبر *دائرة كهربائية خارجية* (سلك) وصولاً إلى المهبط، وهذا التدفق هو ما ينتج التيار الكهربائي [22، 116]. يمكن قياس الفرق في الجهد بين القطبين باستخدام الفولتمتر، ويسمى هذا الفرق *القوة الدافعة الكهربائية* (emf) [119، 121]. *4. جهد الخلية* يُحسب الجهد القياسي لخلية دانيال بطرح جهد القطب القياسي للمصعد من جهد المهبط [25، 127]: جهد النحاس (المهبط) = $+0.34$ فولت. جهد الخارصين (المصعد) = $-0.76$ فولت. *جهد الخلية الكلي ($E^o_{cell}$)* = $0.34 - (-0.76) =$ **$1.10$ فولت**. تعتبر خلية دانيال نموذجاً مثالياً لفهم كيفية عمل البطاريات وإنتاج الطاقة النظيفة من التفاعلات الكيميائية [72، 36]. *#خلية_دانيال* (Daniell Cell) [69، 91] *#الكيمياء_الكهربية* (Electrochemistry) [1، 11] *#الخلايا_الجلفانية* (أو الفولتية) [1، 74، 90] *#الأكسدة_والاختزال* (Redox Reactions) [2، 13، 76] *#الأنود_والمصعد* (قطب الخارصين Zn) [6، 75، 93] *#الكاثود_والمهبط* (قطب النحاس Cu) [6، 75، 93] *#القنطرة_الملحية* (الجسر الملحي) [7، 61، 79] *#القوة_الدافعة_الكهربائية* (E.M.F) [66، 76، 96] *#الرمز_الاصطلاحي* (Cell Representation) [31، 65] *#معادلة_نيرنست* (Nernst Equation) [49، 53] *#جهد_الخلية_القياسي* (1.1 فولت) [32، 67، 96] *#التعادل_الكهربائي* (نقل الأيونات) [7، 62، 84] *#الطاقة_الكيميائية* (تحويلها إلى كهرباء) [1، 69، 74]











![Trump i Netanjahu uderzają. Rosja i Chiny bezsilne [Analiza]](https://imager.clipsaver.ru/NJ0t3ykIjLU/max.jpg)






